
Ihre MIGS-Wahl zählt
Das erste und einzige MIGS-Implantat mit signifikanten Sicherheits- und Wirksamkeitsergebnissen aus einer Zulassungsstudie über 5 Jahre.1,2

Ihre MIGS-Wahl zählt
Das erste und einzige MIGS-Implantat mit signifikanten Sicherheits- und Wirksamkeitsergebnissen aus einer Zulassungsstudie über 5 Jahre.1,2
Hydrus® Microstent:
wegweisende evidenzbasierte Ergebnisse
Der Hydrus® Microstent hat in der „Preferred Practice Pattern“-Leitlinie für das primäre Offenwinkelglaukom der AAO aus dem Jahr 2020 die höchste Datenqualitätsbewertung unter allen MIGS erhalten.3*


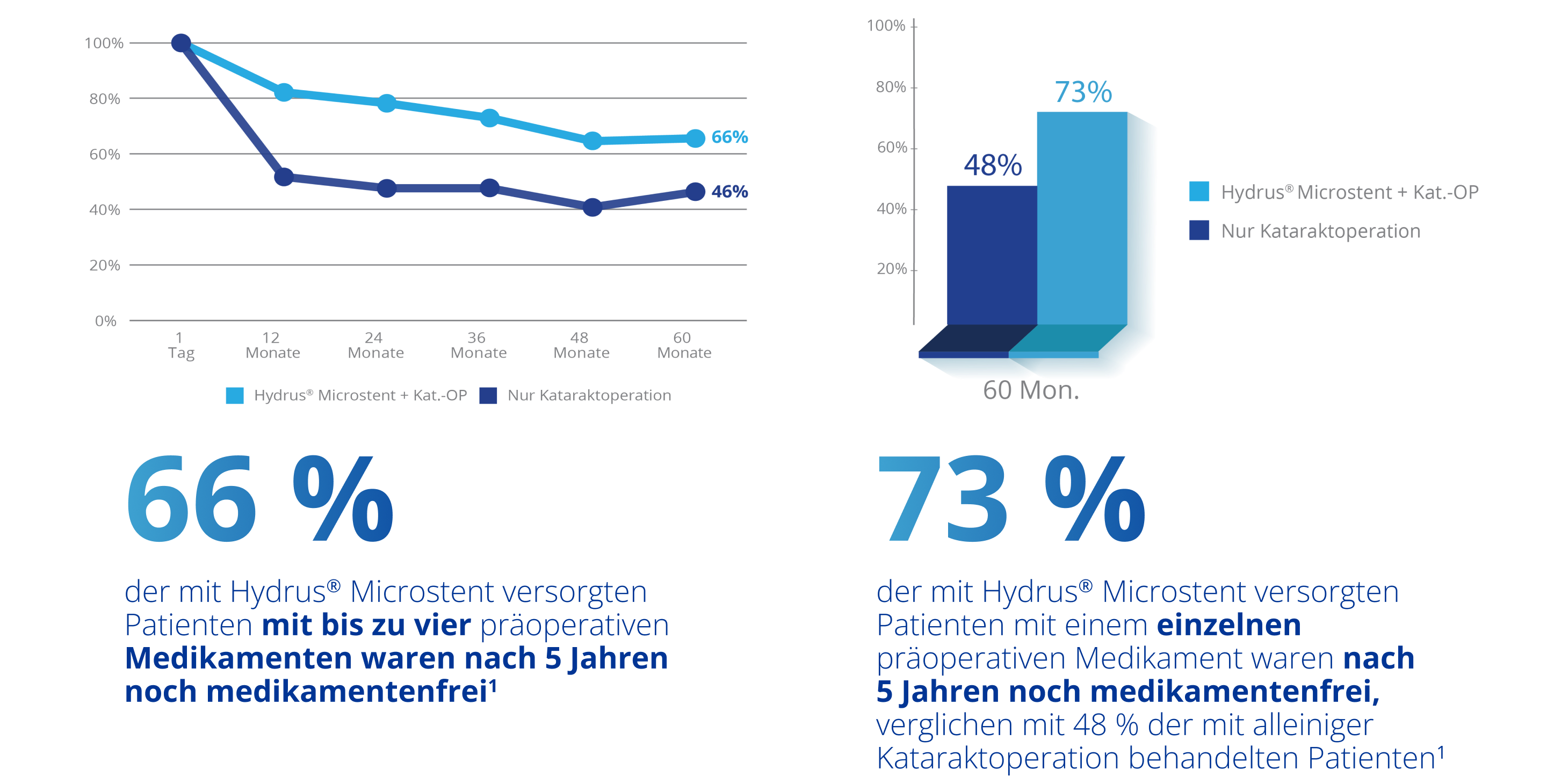
66 % der Hydrus® Microstent Patienten nach 5 Jahren noch medikamentenfrei†

Mehr als 50% relative Reduktion bei inzisionalen SCIs‡ für Hydrus® Microstent Patienten im Vergleich zur alleinigen Katarakt Operation1
(2.4% in Hydrus® + CS vs. 5.3% in CS only)

Überzeugende Langzeitsicherheit nach 60 Monaten mit SUE**-Raten, die mit den Raten bei alleiniger Kataraktoperation vergleichbar sind1,2
Hydrus® Microstent ermöglicht eine sichere und effiziente Microstent-Implantation
Das intuitive Implantationssystem des Hydrus® Microstents gestattet ein unkompliziertes Vorgehen mit sofortiger visueller Bestätigung der erfolgreichen Implantation.
*In der 2020 von der American Academy of Ophthalmology (AAO) herausgegebenen „Preferred Practice Pattern“-Leitlinie für das primäre Offenwinkelglaukom erhielten die Daten zum Hydrus® Microstent die Bewertung „moderate Qualität, starke Empfehlung“ und damit die höchste Bewertung, die unter allen MIGS vergeben wurde
†n = 308 Hydrus® + Kat.-OP
‡Sekundäre chirurgische Intervention (SCI) umfasst Trabekulektomie, Drainage-Implantat, Gel-Stent, ECP/TSCP, nicht-penetrierend; (9/369 Hydrus® und 10/187 Kat.-OP)
**SUE = schwerwiegendes unerwünschtes Ereignis; (13/369 [3,5 %] bei Hydrus® Augen vs. 8/187 [4,3 %] bei den Kontrollaugen)
Innovatives Design und einzigartige Funktionsweise
Mit ungefähr der Größe einer Wimper ist der Hydrus® Microstent ein innovativ, kanalbasiertes MIGS-Implantat für erwachsene Patienten mit leichtem bis moderatem primärem Offenwinkelglaukom.
Das Implantat ist aus Nitinol gefertigt und daher äusserst flexibel und biokompatibel.4



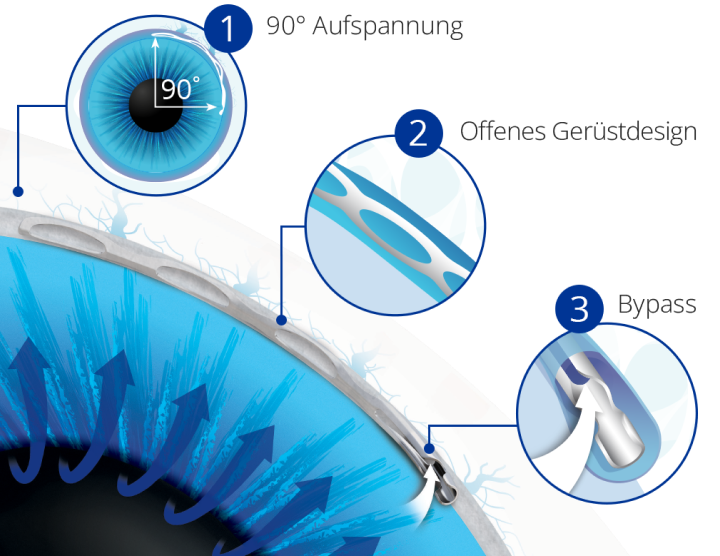
Distal abgerundetes Ende für eine schonende Positionierung in den Schlemm’schen Kanal


Gerüstartiges Design mit Fenstern zur Optimierung des Kammerwasserabflusses


Bypass, der den Abfluss des Kammerwassers von der Vorderkammer in den Schlemm’schen Kanal erleichtert
![]()
90° Aufspannung:
Das einzige MIGS-Implantat, das etwa 90° des Schlemm’schen Kanals aufspannt, sodass der Zugang zu den Kollektorkanälen in der nasalen Region sichergestellt ist.
![]()
Offenes Gerüstdesign:
Das erste MIGS-Implantat zur präzisen Dilatation und Stützung des Schlemm’schen Kanals, das die Querschnittsfläche sanft erweitert, ohne den Zugang zu den Ostien der Kollektorkanäle zu behindern.4
![]()
Bypass:
Der Hydrus® Microstent umgeht das Trabekelmaschenwerk, um den Abluss des Kammerwassers aus der Vorderkammer durch den Einlass des Microstents in den Schlemm’schen Kanal wiederherzustellen.
Wegweisende evidenzbasierte Ergebnisse
Die HORIZON-Studie
Bislang größte prospektive, randomisierte, kontrollierte Zulassungsstudie zu MIGS mit 556 Patienten an 38 Zentren in 9 Ländern und fünf Jahren kontinuierlichem Nachverfolgungsrate mit 80 % im Fünften Jahr.5-8
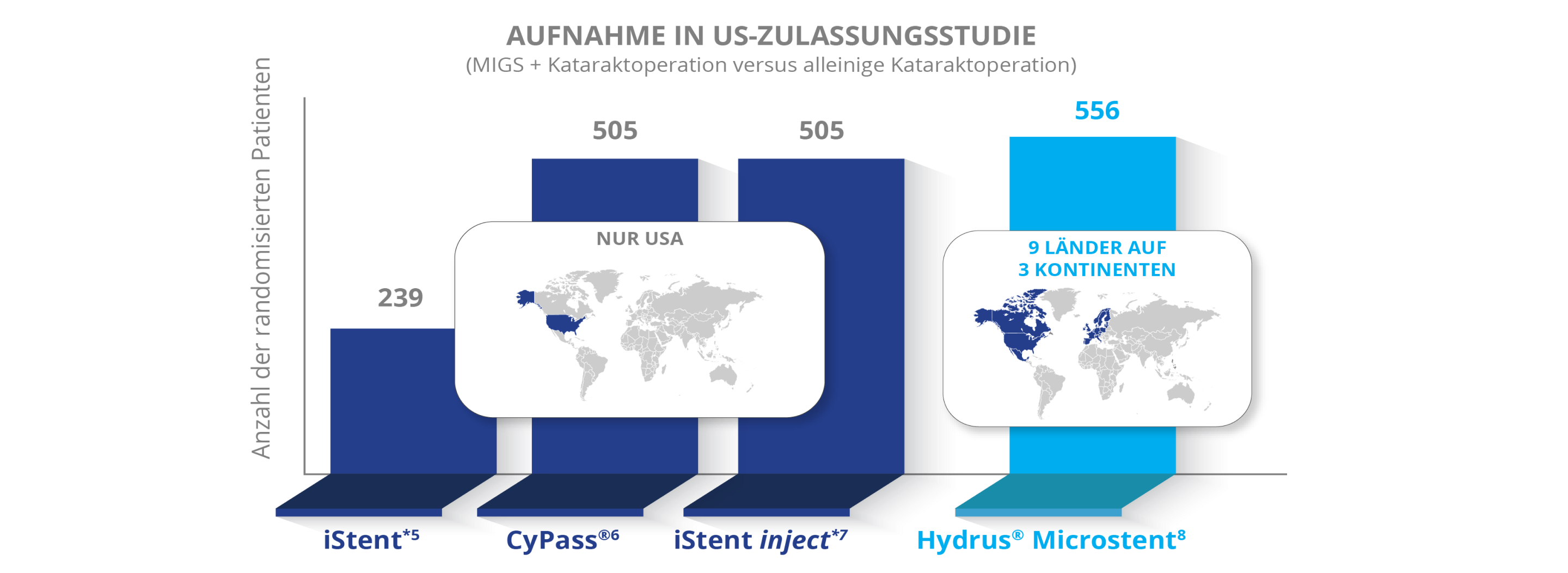
*Marken sind Eigentum ihrer jeweiligen Inhaber.
Klinisch belegte langfristige IOD-Senkung9
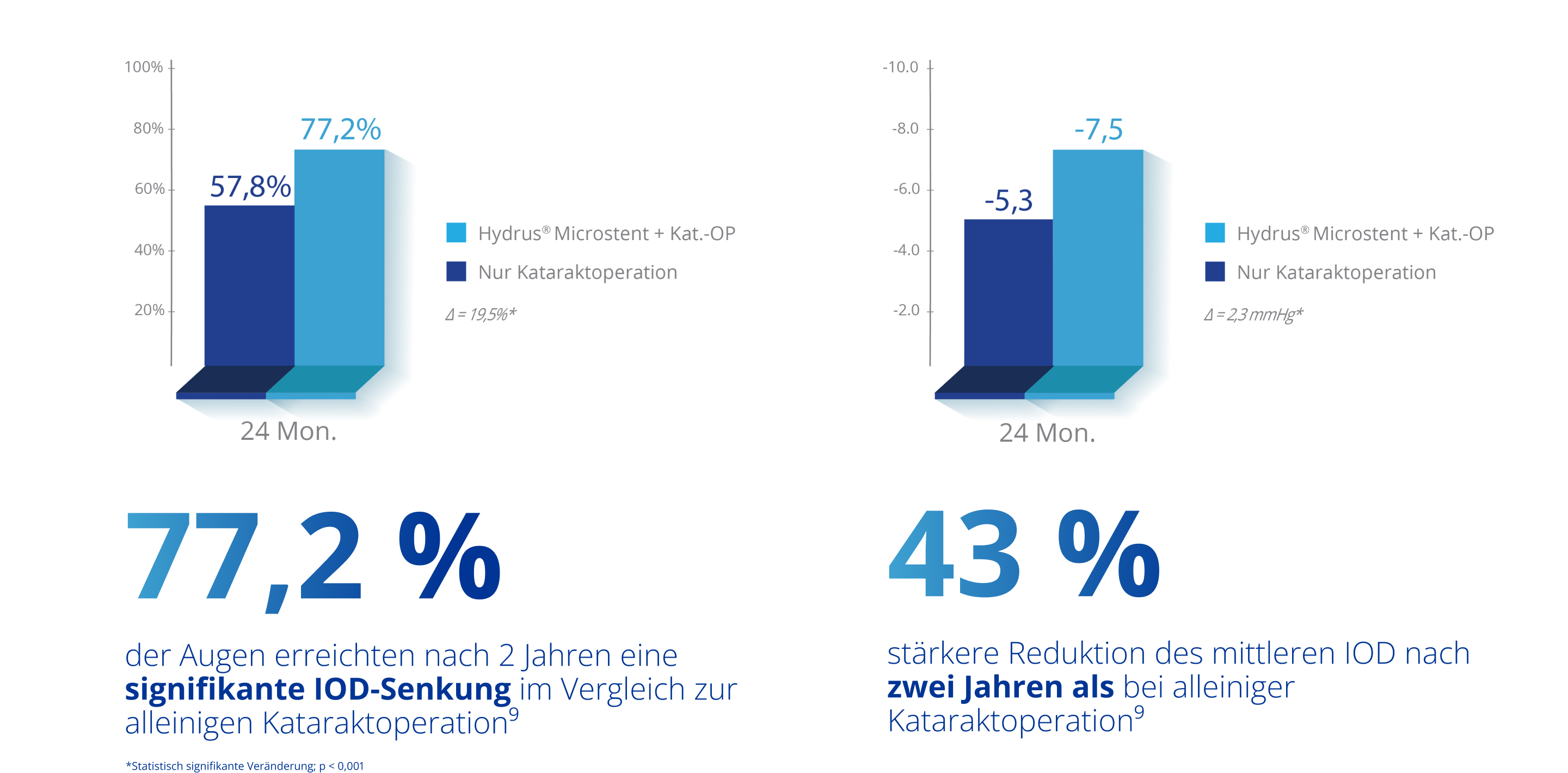
Klinisch belegte langfristige Reduktion der Medikation1,5-7*
Über einen Zeitraum von 5 Jahren war der Prozentsatz inzisionaler SCI* in der Hydrus® Gruppe niedrig1‡
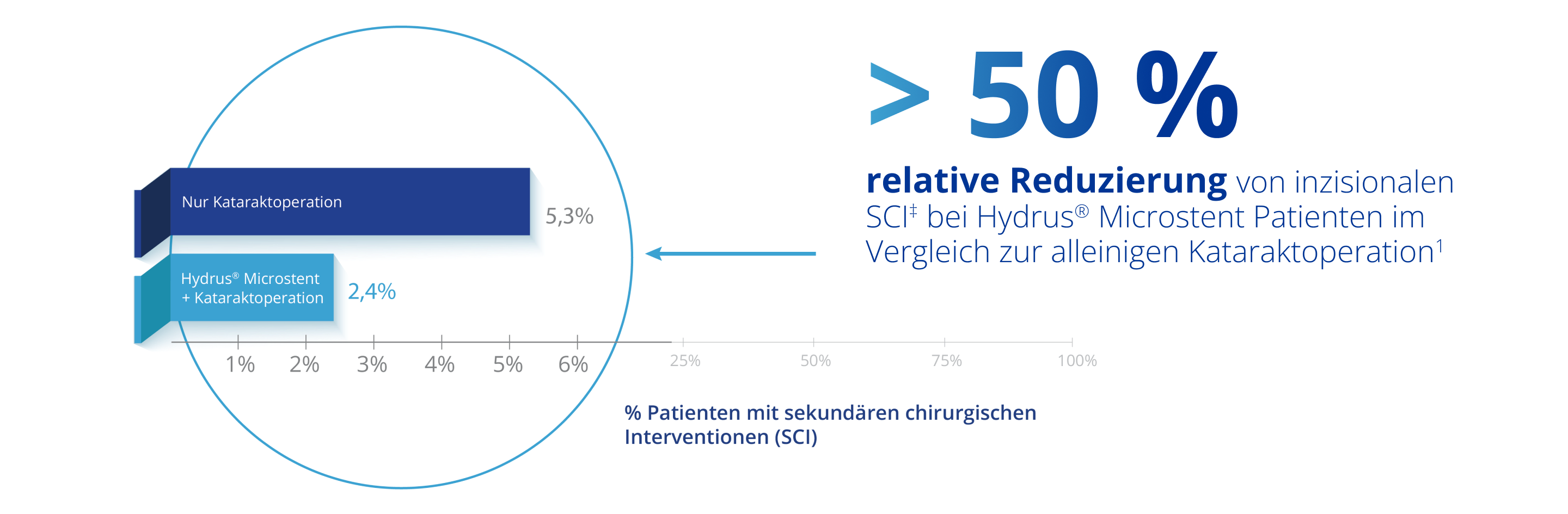
*An den 5 Jahren Follow-up der Zulassungsstudie nahmen 308 Patienten aus der Hydrus® Gruppe und 134 aus der Kontrollgruppe teil.
†Sekundäre chirurgische Intervention (SCI) umfasst Trabekulektomie, Drainage-Implantat, Gel-Stent, ECP/TSCP, nicht-penetrierend; (9/369 Hydrus® und 10/187 Kat.-OP).
Überzeugende Langzeitsicherheit nach 60 Monaten mit SUE*- Raten, die mit den Raten bei alleiniger Kataraktoperation vergleichbar sind1
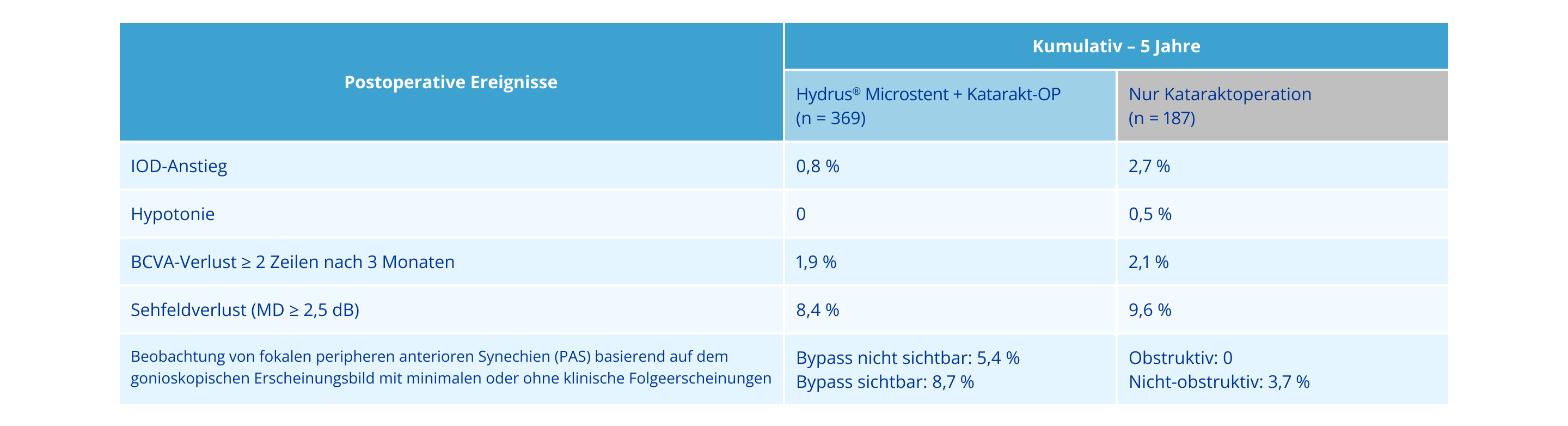
*SUE = schwerwiegendes unerwünschtes Ereignis (13/369 [3,5 %] bei Hydrus®-Augen vs. 8/187 [4,3 %] in der Kontrollgruppe)
Die COMPARE-Studie
Erste prospektive, randomisierte, multizentrische Studie, in der Hydrus® Microstent und 2 iStent* Trabekulären Micro-Bypass Implantate miteinander verglichen wurden
mehr medikamentenfreie Hydrus® Microstent Patienten als medikamentenfreie Patienten mit 2 iStent* Implantaten.10
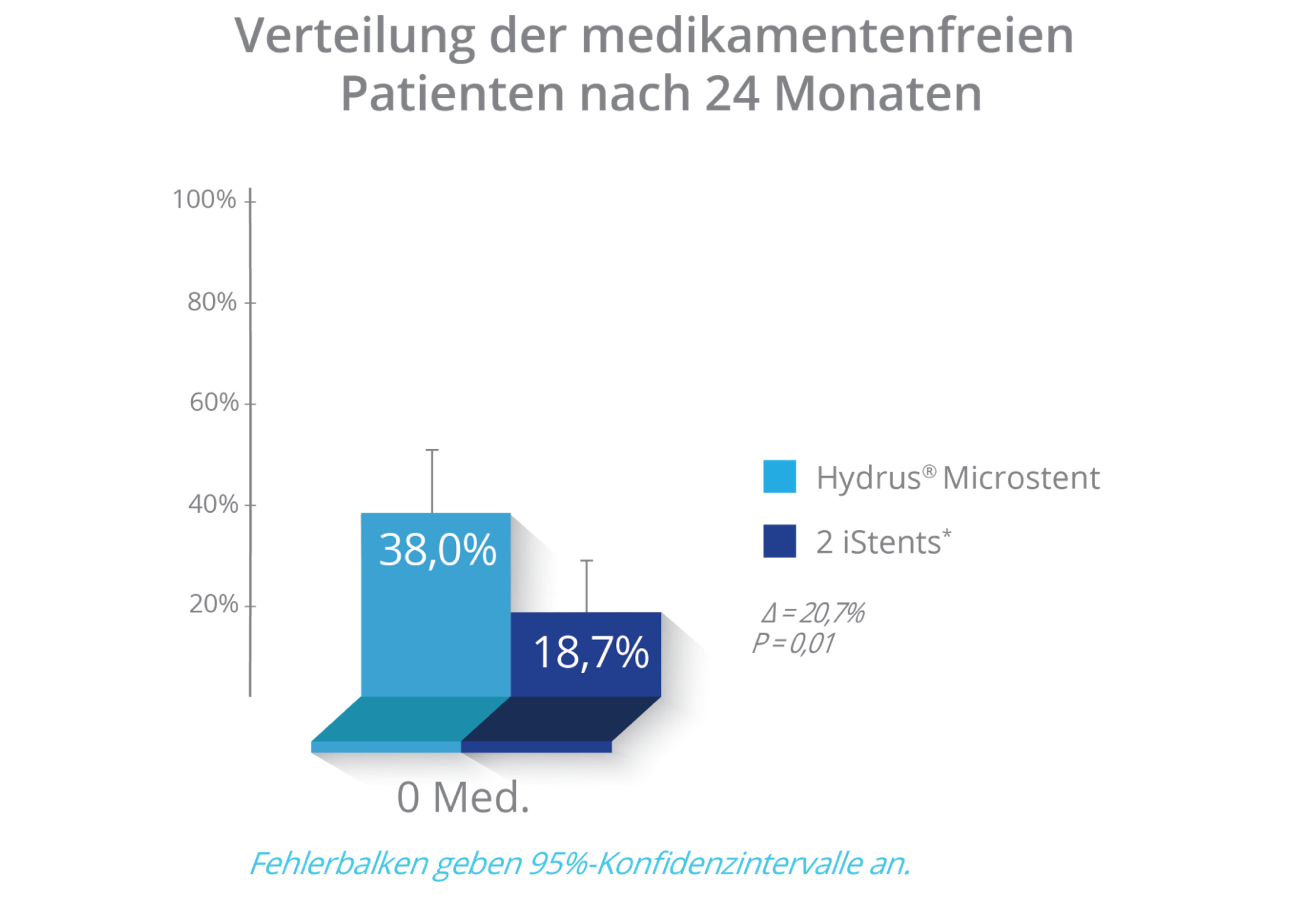

mittlere Verringerung der Medikation nach 2 Jahren mit Hydrus® Microstent, gegenüber 30 % Verringerung in der Gruppe mit 2 iStent*-Implantaten10
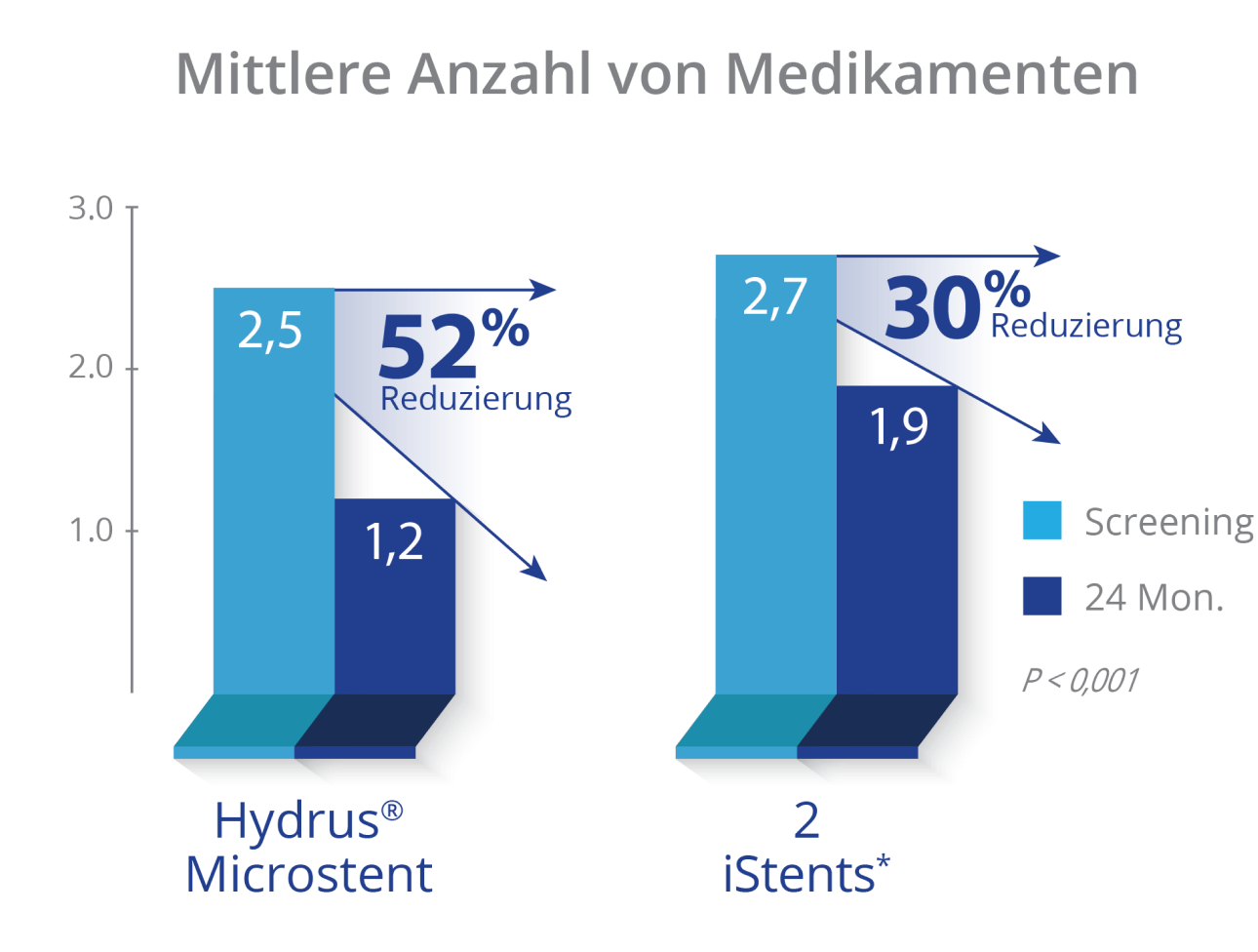
*Marken sind Eigentum ihrer jeweiligen Inhaber.
Anwendung des Hydrus® Microstent in Ihrer Praxis
Entdecken Sie den Hydrus® Microstent
Dr. Ike Ahmed führt eine Hydrus® Microstent-Implantation durch
Klinische Studien zum Hydrus® Microstent
Alcon Experience Academy
Relevante Schulungsinhalte von führenden Branchenvertretern
Literatur:
1. Ahmed IIK, et al. Long-term outcomes from the HORIZON randomized trial for Schlemm’s Canal microstent in combination cataract and glaucoma surgery. Ophthalmology. 2022;129(7):742-751.
2. NIH. Safety & effectiveness study of the Hydrus Microstent for lowering IOP in glaucoma patients undergoing cataract surgery (HORIZON). ClinTrials.gov (NCT01539239).
3. Gedde SJ, et al. Primary open-angle glaucoma preferred practice pattern. Ophthalmology 2020;128(1): 71-150.
4. Hydrus Microstent Gebrauchsanweisung. 2020.
5. US Food & Drug Administration. Summary of Safety and Effectiveness Data (SSED): Glaukos iStent® Trabecular Micro-Bypass Stent. https://www.accessdata.fda.gov/cdrh_docs/pdf8/P080030B.pdf. Veröffentlicht am 25. Juni 2012.
6. US Food & Drug Administration. Summary of Safety and Effectiveness Data (SSED): CyPass System. https://www.accessdata.fda.gov/cdrh_docs/pdf15/P150037B.pdf. Veröffentlicht am 29. Juli 2016.
7. US Food & Drug Administration. Summary of Safety and Effectiveness Data (SSED): iStent inject Trabecular Micro-Bypass System. https://www.accessdata.fda.gov/cdrh_docs/pdf17/P170043b.pdf Veröffentlicht am 21. Juni 2018.
8. US Food & Drug Administration. Summary of Safety and Effectiveness Data (SSED): CyPass System. Hydrus Microstent. https://www.accessdata.fda.gov/cdrh_docs/pdf17/P170034B.pdf. Veröffentlicht am 10. August 2018.
9. Samuelson TW, Chang DF, Marquis R, et al. A Schlemm canal microstent for intraocular pressure reduction in primary open-angle glaucoma and cataract: The HORIZON Study. Ophthalmology. 2019;126:29-37.
10. Daten im Alcon-Archiv, 2018.
11. Otarola F, Virgili G, Shah A, et al. Ab interno trabecular bypass surgery with Schlemm ́s canal microstent (Hydrus) for open angle glaucoma. Cochrane Database of Systematic Reviews. 2020;3:CD012740.
Die vollständige Liste mit Indikationen, Kontraindikationen und Warnhinweisen finden Sie in der jeweiligen Gebrauchsanweisung.




